Introducción
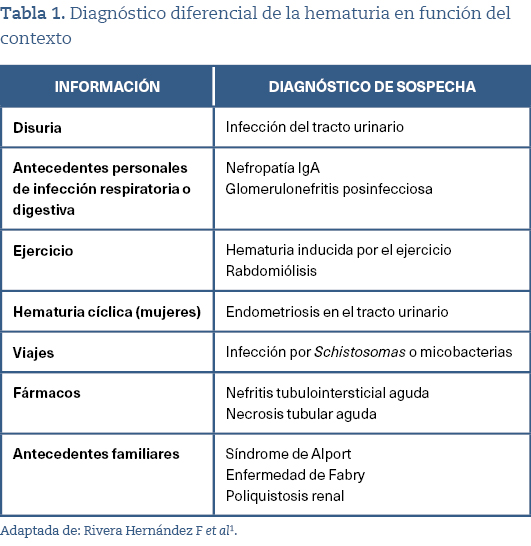
La hematuria se define como la presencia de hematíes en la orina. Se distingue entre microhematuria (aspecto normal) y macrohematuria (el color puede variar entre rojo y marrón oscuro). El abordaje diagnóstico-etiológico depende de diversos factores (tabla 1)1.
Las series americanas cifran la prevalencia de hematuria entre el 2,1 y el 31,4%. Suele ser secundario a neoplasias de vía urinaria. También puede deberse a infecciones, fármacos o tóxicos, exposición a agentes químicos, etc. Una prueba útil es la determinación con tiras reactivas de orina, aunque, sustancias como el hipoclorito de sodio (lejía) o ciertas peroxidasas vegetales pueden dar un falso positivo. El gold standard es el sedimento urinario2.
La mesalazina pertenece al grupo de fármacos que contiene ácido 5-aminosalicílico (5-ASA). El 28% de ella es absorbido en el tubo digestivo y se elimina por el riñón. El riesgo de aparición de nefritis intersticial por reacción de hipersensibilidad es infrecuente. Datos del Reino Unido cifran la incidencia de enfermedad renal asociada en 0,17 casos por 100 pacientes-año3.
La correcta filiación de antecedentes, la comprobación de los hallazgos y su diagnóstico diferencial inicial son parte de la consulta diligente en Atención Primaria (AP), pero requieren de un manejo combinado con nefrología si existe sospecha de patología subyacente o de una entidad secundaria a fármacos.
Caso clínico
Mujer de 24 años con alteración de la coloración de la orina.
Antecedentes personales: intolerancia digestiva a amoxicilina/ácido clavulánico.
Antecedentes familiares: padre con microhematuria persistente no biopsiada.
Cronograma:
- Episodio de orina color refresco de cola sin clínica miccional. Valorada en punto de atención continuada (PAC), donde se pauta fosfomicina.
- Vuelve a presentar coluria 15 días después y se realiza tira reactiva de orina en el centro de salud (CS): pH: 6,0; densidad: 1.015; cuerpos cetónicos. El urocultivo resulta negativo, y el sedimento, sin hematuria. Albuminuria libre (MAL): 0,3 mg/dl.
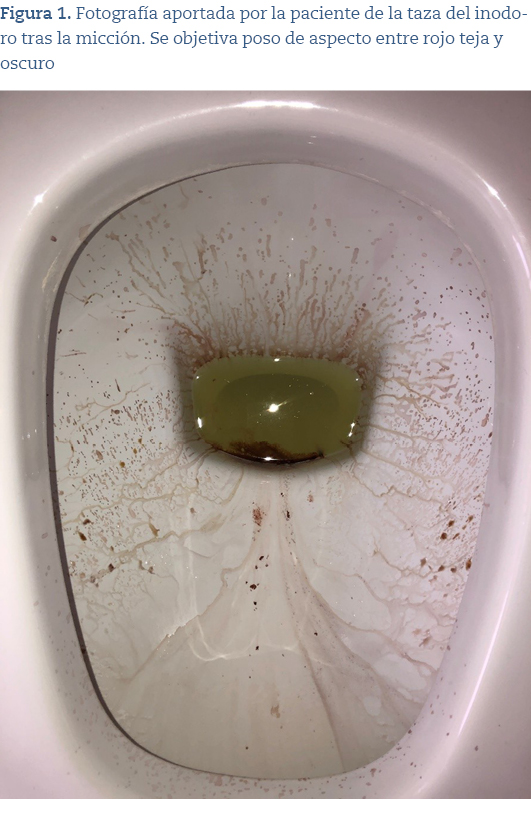
- Tras otros 5 días, presenta un nuevo episodio de orina marronácea-anaranjada y poso sobre taza del inodoro (figura 1). Acude al PAC y se realiza tira reactiva (sangre ++++, cuerpos cetónicos ++++, proteínas ++++). Es derivada al servicio de urgencias hospitalario (SUH), donde se realiza anormales y sedimento con presencia de hematíes 250/µl y 10-25 hematíes por campo.
- Un mes después del primer evento, su especialista en Medicina Familiar y Comunitaria (MFyC) contacta con nefrología para valoración conjunta y 4 meses más tarde se cita a la paciente en consulta de Nefrología con estudio analítico completo. Presentaba función renal conservada, sedimento y albuminuria normales, bioquímica hepática, hemograma y estudio básico de autoinmunidad sin alteraciones (Cr 0,79 mg/dl; filtrado glomerular estimado [FGe] 104 ml/min/1,73 m2; MAL 0,3 mg/dl; proteinograma C3 y C4 y anticuerpos antinucleares en rango de normalidad; anticuerpos antitransglutaminasa [IgA] 7,5; velocidad de sedimentación globular 16 mm). Tras revisar su historia clínica, se observa un ingreso a cargo de medicina digestiva por diarrea, en el que se detectó Campylobacter jejuni, y recibió el alta once días antes de la aparición del primer episodio de orina color refresco de cola. En la colonoscopia, se objetivaron datos de colitis de distribución parcheada (probable enfermedad de Crohn), por lo que se tomaron biopsias y se inició tratamiento con mesalazina 15 días antes de la alteración del aspecto de la orina.
- Proceso diagnóstico: se amplía estudio con ecografía renal y nuevo estudio analítico incluyendo analítica de orina de 24 horas con oxalato, citrato, urato y calcio
- Juicio clínico y diagnóstico diferencial: alteraciones del aspecto macroscópico de la orina en probable contexto de tratamiento con mesalazina frente a macrohematuria aislada.
- Plan: se contacta con medicina digestiva para valorar retirada de mesalazina.
- Evolución: la paciente mantiene el tratamiento durante casi 1 año. Tras la retirada del fármaco, no ha vuelto a aparecer la clínica. No se objetivaron alteraciones en las pruebas complementarias solicitadas.
Discusión
La sensibilidad para detectar hematuria de las tiras de orina es del 100%, con una especificidad del 65-99%. Existen limitaciones, como la contaminación con soluciones antisépticas oxidantes (falso positivo) o el tratamiento con captopril o vitamina C (falso negativo). Una tira de orina positiva obliga a confirmar el resultado (sedimento)4.
Existen casos de modificaciones del color de la orina con el tratamiento con mesalazina. Se trata de cambios en el aspecto de la orina al contactar con el agua del inodoro tras haber limpiado con lejía. Un chico de 16 años comenzó con hematuria/coluria tras 3 años de tratamiento con mesalazina (asintomático)5. Otro hombre de 38 años, con enfermedad de Crohn y en tratamiento con mesalazina, inició episodios de coluria, y una mujer de 36 años, con colitis ulcerosa y en tratamiento con mesalazina, asoció dolor abdominal con las crisis de hematuria/coluria6.
La mesalazina se acetila en ácido N-acetil-5-mesalazina a través de la enzima N-acetil-transferasa 1 (NAT1). Existen polimorfismos de esta enzima que conllevan diferentes niveles de actividad. Se trabaja sobre la hipótesis de que niveles de actividad traen consigo diferentes formas de excreción que puedan alterar el aspecto de la orina7.
Un estudio de solubilidad de la mesalazina ha objetivado que esta precipita a un pH menor (entre 2 y 6). Factores asociados a la enfermedad inflamatoria intestinal, como la diarrea (disminución de volumen) y la orina concentrada, pueden aumentar el riesgo de precipitación8.
Los protocolos de evaluación de hematuria desde AP se centran en filiar la causa de la misma:
- Comprobar la hematuria mantenida (repitiendo el análisis en el plazo de 3-4 semanas).
- Descartar infección.
- Valorar su relación con factores externos (ejercicio físico, traumatismos, procesos febriles, consumo de fármacos/tóxicos, etc.).
- Valorar la presencia de alteraciones en el sedimento (cilindros, proteinuria, etc.).
- Determinar la función renal y descartar insuficiencia renal.
En función de estos datos, se procederá a la solicitud de pruebas de imagen, siendo la más rentable la ecografía de vías urinarias y vejiga9.
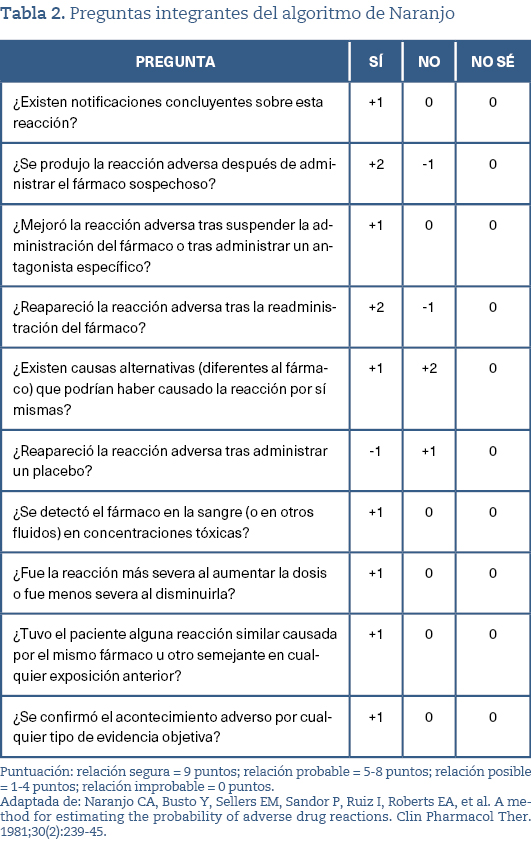
Es importante el proceso de identificación de eventos adversos de los fármacos, con lo que cobra importancia el algoritmo de Naranjo (tabla 2). Se debe tener en cuenta la asociación temporal y hay que basarse en estrategias que aporten evidencia y refuercen la sospecha. También debe evaluarse la respuesta clínica tras la retirada del mismo10.
Se calculó la puntuación de Naranjo con 5 puntos (relación probable):
- Sí existen notificaciones sobre esta reacción en la evidencia (tres casos a nivel mundial) y hay datos de polimorfismo de actividad de la enzima que pueden explicar la etiopatogenia (+1 punto).
- Se produjo la reacción adversa tras el inicio del fármaco (+2 puntos).
- Mejoró la situación tras la retirada de la mesalazina (+1 punto).
- Existen causas alternativas al fármaco (+1 punto).
Es importante tener en cuenta que, en casos atípicos como el expuesto, debemos descartar la afectación renal aguda y tratar hipótesis diagnósticas hasta llegar a un diagnóstico de certeza, teniendo en cuenta la situación clínica del paciente. El trabajo combinado de especialistas en MFyC y nefrología es fundamental para alcanzar un manejo diligente.
Agradecimientos
Se obtuvo el consentimiento firmado de la paciente para la publicación del artículo.
Consideraciones
Se han tenido en cuenta las recomendaciones del CARE Statement en la redacción de este caso clínico.
Financiación
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro, formando parte de la asistencia clínica en consulta diaria. El manejo de la paciente se ha llevado a cabo de acuerdo con los criterios del Médico Responsable y las evidencias científicas derivadas de la práctica clínica diaria. El caso clínico, así como la labor asistencial descrita, cumple con los requisitos de la Declaración de Helsinki para investigación en humanos. Se ha llevado a cabo la descripción del caso clínico y el manejo de datos según las guías de buena práctica clínica.
Conflicto de intereses
El caso clínico descrito no se ha presentado en ninguna otra actividad (congreso, talleres, sesiones clínicas…) ni ha sido remitido para evaluación por otras revistas científicas.
El autor principal y los autores colaboradores declaran no tener conflictos de interés ni con la Revista Clínica de Medicina de Familia ni con la industria farmacéutica en relación con la valoración del artículo.
El autor principal pertenece al Consejo Editorial de la Revista FML (Societat Valenciana de Medicina Familiar i Comunitaria [SoVaMFiC]) como revisor científico y maquetador.
El doctor Pablo José Sanz Navarro, el doctor José Rodríguez Contreras y la doctora Susana Cruz Maeso son socios federados de la Sociedad Española de Medicina de Familia y Comunitaria (semFYC) y el doctor Joaquín de Juan Ribera es socio de la Sociedad Española de Nefrología.
El doctor Pablo José Sanz Navarro colabora con GSK (GlaxoSmithKline, S.A.) en la actividad Workshop con residentes de Atención Primaria, Pediatría y Urgencias.