Introducción
El síndrome miasteniforme de Eaton Lambert (Lambert-Eaton myasthenic syndrome, LEMS) es un trastorno autoinmune basado en la producción de autoanticuerpos contra los canales de calcio voltaje dependientes de la unión neuromuscular1.
El 60% de los pacientes con LEMS presentan un proceso oncológico subyacente, siendo el carcinoma de pulmón de células pequeñas (small cell lung cancer, SCLC) el más frecuentemente asociado2. El LEMS es el tercer síndrome paraneoplásico en frecuencia, solo por detrás del síndrome de secreción inadecuada de ADH y del síndrome de Cushing2. Su presentación suele preceder en meses al diagnóstico del tumor1, por lo que es fundamental reconocer esta entidad poco común, siendo Atención Primaria el ámbito en el que los pacientes suelen consultar en primer lugar.
Caso clínico
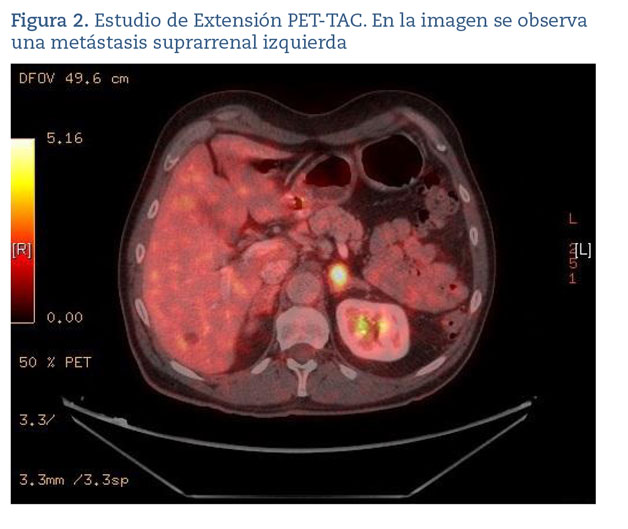
Presentamos el caso de un hombre de 60 años con múltiples antecedentes cardiológicos (fibrilación auricular paroxística, cardiopatía hipertensiva, aneurisma de aorta y angina de esfuerzo) que acude a consulta de seguimiento por cardiología y refiere debilidad progresiva de predominio proximal en miembros inferiores de 3 meses de evolución. Previamente había consultado por el mismo motivo a su médico de Atención Primaria y en dos ocasiones en el servicio de urgencias, habiendo interpretado los síntomas en el contexto de astenia de origen multifactorial. Como parte del estudio cardiovascular, se realiza una angiotomografía computarizada (angio-TC) de arterias coronarias donde se identifica, como hallazgo incidental, un nódulo pulmonar LII (CAD-RADs1) que histológicamente se corresponde con un carcinoma de pulmón de células pequeñas. En el estudio de extensión se identifican adenopatías y una metástasis suprarrenal izquierda (cTxN2M1b) (figuras 1 y 2).
En cuanto a la debilidad de miembros inferiores, el paciente describe que empeora al subir escalones y conforme avanza el día. Es indolora y no se asocia a claudicación ni a déficits neurológicos focales. Se realiza eco-Doppler, que corrobora una adecuada perfusión vascular, y se solicita estudio electromiográfico (EMG), que no resulta concluyente (figura 3). Finalmente, en el estudio de autoinmunidad los anticuerpos anticanales de calcio voltaje dependientes resultan positivos. Se trata de un LEMS paraneoplásico en el contexto de un SCLC.
Se inicia tratamiento con 3,4 diaminopiridina, que se suspende tras 3 meses por falta de respuesta y molestias gástricas; posteriormente, se administra piridostigmina, también ineficaz, y finalmente se planifican ciclos de inmunoglobulinas intravenosas a dosis de 0,4 g/kg/día durante 5 días. Respecto al tratamiento oncológico, se inicia esquema de quimioterapia con carboplatino + etopósido (6 ciclos) junto con radiografía torácica y suprarrenal izquierda en esquema de 30 Gy en 10 fracciones en cada localización. Hasta la fecha, 1 año y 6 meses tras el inicio de la quimioterapia, el paciente se mantiene en remisión completa sin haber vuelto a presentar brotes de LEMS desde el alcance de la remisión tumoral.
Discusión
Ante un cuadro de debilidad muscular, tras descartar causas farmacológicas (corticoides, cloroquina) y endocrinológicas (como el síndrome de Cushing o las alteraciones tiroideas), se debe establecer el diagnóstico diferencial entre neuropatías, miopatías y trastornos de la placa motora.
Mientras que las neuropatías se caracterizan por debilidad muscular distal y amiotrofia, las miopatías y los trastornos de la placa motora cursan con debilidad proximal, que, en el caso de los trastornos de la placa motora, como el LEMS, se acompaña además de fatigabilidad3.
El LEMS se caracteriza por debilidad muscular proximal en extremidades que progresa en sentido caudo-craneal, disautonomía y arreflexia. El diagnóstico diferencial debe establecerse principalmente con la miastenia gravis (MG) (afectación precoz de la musculatura oculobulbar, progresión cráneo-caudal, sin arreflexia ni disautonomía)3 y el botulismo (arreflexia, disautonomía y evolución a parálisis bulbar y flácida)4.
Se debe hacer una EMG con estimulación repetitiva (que origina una disminución del potencial en la MG y un ascenso en el LEMS)5 y un estudio de autoinmunidad. Los anticuerpos antirreceptores de acetilcolina y anti-Musk son típicos de la MG, mientras que los anticuerpos anticanales de calcio de tipo P/Q se encuentran casi en el 100% de los pacientes con LEMS con asociación tumoral y en el 90% de los LEMS sin dicha asociación2.
Hasta en un 60% de los casos, el LEMS constituye un síndrome paraneoplásico que se suele manifestar meses antes de que el cáncer subyacente se evidencie clínicamente, de ahí la importancia de reconocerlo6. De estos, la mitad se deben a un SCLC. Sin embargo, la literatura recoge diversos casos de LEMS asociados a otros tipos de tumores, en especial de próstata, timo, laringe y algunos síndromes linfoproliferativos. Cabe destacar que en el análisis anatomopatológico de la mayoría de los tumores asociados a LEMS se encontraron características celulares neuroendocrinas y que la actividad tumoral se pudo correlacionar con la actividad del síndrome paraneoplásico7. Por tanto, al igual que sucede en el caso presentado, al alcanzar la remisión completa, remiten los síntomas de LEMS, de manera que un brote de debilidad muscular debe hacer sospechar recidiva tumoral. Si esta situación se presenta en Atención Primaria, se debe derivar lo antes posible al medio hospitalario.
De los pacientes con SCLC, aquellos en los que el tumor se asocia al LEMS presentan mayor supervivencia debido probablemente a un diagnóstico más precoz de la enfermedad oncológica8.
En cuanto al tratamiento del LEMS, la remisión completa del proceso oncológico suele conllevar su desaparición. Mientras, como medidas encaminadas al alivio sintomático, se emplean la 3,4-diaminopirimidina y la piridostigmina como primera línea y, al igual que en nuestro caso, la terapia con inmunoglobulinas intravenosas como segundo escalón en casos refractarios9.
En resumen, el manejo del LEMS precisa de un abordaje multidisciplinar que comienza con la sospecha precoz en el ámbito de la Atención Primaria. Identificarlo adelanta el diagnóstico oncológico y mejora la supervivencia. La actividad del LEMS suele ser paralela a la actividad tumoral, por lo que, ante el reinicio de los brotes en un paciente en remisión tumoral completa, se debe derivar precozmente a medio hospitalario bajo la sospecha de recidiva de la enfermedad oncológica.
Agradecimientos
Se obtuvo el consentimiento escrito del paciente para la publicación del manuscrito.